Ensüümid
määratlus
Ensüümid on keemilised ained, mida võib leida kogu kehas. Nad seovad kehas keemilisi reaktsioone.
ajalugu
Sõna ensüüm oli pärit Wilhelm Friedrich Kühne 1878 ja on tuletatud kreekakeelsest sõnast ensmon, mis tähendab pärmi või haput. See leidis siis tee rahvusvahelisse teadusesse. puhta rakenduskeemia rahvusvaheline liit (IUPAC) ja rahvusvaheline biokeemiate liit (IUBMB) töötas välja ensüümide nomenklatuuri, mis määratleb selle suure ainete rühma esindajad ühise rühmana. Nimetamine, mis klassifitseerib ensüümid vastavalt nende ülesandele, on oluline üksikute ensüümide ülesannete kindlaksmääramisel.
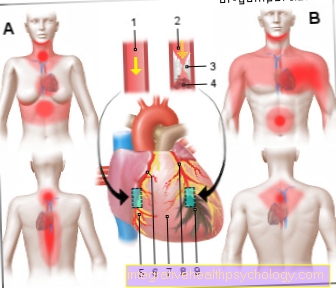
Ensüümide illustratsioon
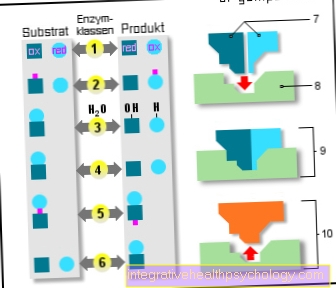
Ensüümid
6 ensüümiklassi:
- Oksidoreduktaasid
(Oksüdeerimine / redutseerimine) - Transferaasid
(Edasikandumine) - Hüdrolaasid
(Vee kasutamine) - Lüase
(Lõhkumine) - Isomeraasid
(sama molekulaarne valem) - Ligases
(Täiendavad reaktsioonid) - Aluspinnad
- Aktiivne keskus
- Ensüüm / substraat
keeruline - Ensüüm / toode
keeruline
Ülevaade kõigistDr-Gumperti pildid leiate aadressilt: meditsiinilised illustratsioonid
Nimetamine
Nimetamine ensüüm on sisse lülitatud kolm peamist põhimõtet põhinev.Ensüümide nimed, mis lõpevad inaasiga, kirjeldavad süsteemi mitut ensüümi. Ensüümi nimetus ise kirjeldab reaktsiooni, mille ensüüm käivitab (katalüüsitud). Ensüümi nimi on ka ensüümi klassifikatsioon. Lisaks koodisüsteem, mis EÜ numbrite süsteem, milles ensüümid valmistatakse numbrilise koodi all neli numbrit leitav. Esimene number tähistab ensüümi klassi. Kõigi tuvastatud ensüümide loendid tagavad kindlaksmääratud ensüümi koodi kiirema leidmise. Ehkki koodid põhinevad ensüümi katalüüsitava reaktsiooni omadustel, osutuvad numbrilised koodid praktikas raskeks. Ülaltoodud reeglitel põhinevaid süstemaatilisi nimesid kasutatakse sagedamini. Nomenklatuuriga tekivad probleemid näiteks ensüümidega, mis katalüüsivad mitmeid reaktsioone. Seetõttu on neil mõnikord mitu nime. Mõnel ensüümil on triviaalsed nimed, mis ei näita, et nimetatud aine on ensüüm. Kuna nimesid kasutati traditsiooniliselt laialt, säilitati mõned neist.
Klassifikatsioon vastavalt ensüümi funktsioonile
IUPAC ja IUBMB andmetel jagunevad ensüümid kuue ensüümiklassi vastavalt nende algatatud reaktsioonile:
- Oksidoreduktaasid
Oksidoreduktaasid panid liikuma redoksreaktsioonid. Selles keemilises reaktsioonis liiguvad elektronid ühelt reaktsioonipartnerilt teisele. Toimub ühe aine elektronide vabanemine (oksüdeerumine) ja teise aine elektronide omastamine (redutseerimine).
Katalüüsitud reaktsiooni valem on A + + APa + AP.
Aine A vabastab elektroni (?) Ja oksüdeeritakse, samas kui aine B neelab selle elektroni ja redutseeritakse. Seetõttu nimetatakse redoksreaktsioone ka redutseerimise-oksüdatsiooni reaktsioonideks.
Paljud metaboolsed reaktsioonid on redoksreaktsioonid. Oksügenaasid viivad substraadile ühe või mitu hapnikuaatomit. - Transferaasid
Transferaasid viivad funktsionaalrühma ühest substraadist teise. Funktsionaalrühmad on orgaaniliste ühendite aatomirühmad, mis määravad suures osas aine omadused ja reaktsiooni käitumise. Keemilised ühendid, millel on samad funktsionaalrühmad, on sarnaste omaduste tõttu rühmitatud ainerühmadeks. Funktsionaalrühmad jagatakse vastavalt sellele, kas nad on heteroaatomid või mitte. Heteroaatomid on kõik orgaaniliste ühendite aatomid, mis ei ole süsinik ega vesinik.
Näide: -OH -> hüdroksüülrühm (alkoholid) - Hüdrolaasid
Hüdrolaasid lõhestavad sidemeid veega kasutades pöörduvates reaktsioonides. Estrid, estrid, peptiidid, glükosiidid, happeanhüdriidid või C-C sidemed. Tasakaaluline reaktsioon on: A-B + H2O? A-H + B-OH.
Hüdrolaaside rühma kuuluv ensüüm on nt. Alfa-galaktosidaas. - Lüase
Lüaasid, mida nimetatakse ka süntaasideks, katalüüsivad keerukate saaduste lõhustumist lihtsatest substraatidest ilma ATP-d lõhestamata. Reaktsiooniskeem on A-B → A + B.
ATP on adenosiintrifosfaat ja nukleotiid, mis koosneb nukleosiidi adenosiini trifosfaadist (ja sellisena nukleiinhappe RNA energiarikas ehitusplokk). Kuid ATP on peamiselt igas rakus kohe saadaval oleva energia universaalne vorm ja samal ajal oluline energiavarustusprotsesside regulaator. Vajadusel sünteesitakse ATP teistest energiavarudest (kreatiinfosfaat, glükogeen, rasvhapped). ATP molekul koosneb adeniinijääkidest, suhkru riboosist ja kolmest fosfaadist (a kuni?) Estri (a) või anhüdriidsidemetest (a ja a). - Isomeraasid
Isomeraasid kiirendavad isomeeride keemilist muundamist. Isomeeria on kahe või enama täpselt samade aatomitega (sama empiiriline valem) ja molekulmassiga keemiliste ühendite esinemine, mis erinevad siiski aatomite ühenduses või ruumilises paigutuses. Vastavaid ühendeid nimetatakse isomeerideks.
Need isomeerid erinevad oma keemiliste või / ja füüsikaliste ning sageli ka biokeemiliste omaduste poolest. Isomeeria toimub peamiselt orgaaniliste ühenditega, aga ka (anorgaaniliste) koordinatsioonühenditega. Isomeeria jaguneb erinevatesse piirkondadesse. - Ligases
Ligaasid katalüüsivad selliste ainete moodustumist, mis on keemiliselt keerukamad kui kasutatavad substraadid, kuid vastupidiselt lüasidele on ATP lõhustamisel ensümaatiliselt tõhusad. Nende ainete moodustumine nõuab seetõttu energiat, mis saadakse ATP poolitamise teel.
Mõned ensüümid on võimelised katalüüsima mitmeid, mõnikord väga erinevaid reaktsioone. Kui see on nii, määratakse nad mitmesse ensüümiklassi.
Teid võivad huvitada ka need artiklid:
- Alfa-glükosidaas
- Lipaas
- Trüpsiin
Klassifikatsioon vastavalt ensüümi struktuurile
Peaaegu kõik ensüümid on valgud ja neid saab liigitada vastavalt valguahela pikkusele:
- Monomeerid
Ensüümid, mis koosnevad ainult ühest valguahelast - Oligomeerid
Ensüümid, mis koosnevad mitmest valguahelast (monomeerid) - Mitme ensüümi ahelad
Mitmed agregeeritud ensüümid, mis teevad koostööd ja reguleerivad üksteist. Need ensüümiahelad katalüüsivad raku ainevahetuse järjestikuseid etappe.
Lisaks on üksikud valguahelad, mis sisaldavad mitmeid ensüümide aktiivsusi, neid nimetatakse multifunktsionaalseteks ensüümideks.
Klassifikatsioon vastavalt kofaktoritele
Teine klassifikatsioon on klassifikatsioon vastavalt kofaktorite kaalutlustele. Kofaktorid, koensüümid ja kaassubstraadid on ainete erinevad klassifikatsioonid, mis mõjutavad ensüümidega interaktsiooni kaudu biokeemilisi reaktsioone.
Arvesse võetakse orgaanilisi molekule ja ioone (enamasti metalliioone).
Puhtad valguensüümid koosnevad eranditult valkudest ja aktiivne keskus moodustatakse ainult aminohappejääkidest ja peptiidi karkassist. Aminohapped on orgaaniliste ühendite klass, milles on vähemalt üks karboksürühm (-COOH) ja üks aminorühm (-NH2).
Holoensüümid koosnevad valgukomponendist, apoensüümist ja kofaktorist, madala molekulmassiga molekulist (mitte valgust). Mõlemad koos on ensüümi funktsioneerimiseks olulised.
Koensüümid
Orgaanilisi molekule kui kofaktoreid nimetatakse koensüümideks. Kui nad on apoensüümiga kovalentselt seotud, nimetatakse neid proteesirühmadeks või kaassubstraatideks. Proteesirühm on termin, mida kasutatakse valguvabade komponentide kirjeldamiseks, mis on kindlalt (tavaliselt kovalentselt) seotud katalüütilise toimega valguga.
Kosubstraadid on mitmesuguste ainete klassifikatsioonide nimetused, mis mõjutavad biokeemilisi reaktsioone ensüümide interaktsiooni kaudu. Biokatalüsaatoritena kiirendavad molekulid organismides reaktsioone, ensüümid kiirendavad biokeemilisi reaktsioone. Need vähendavad aktiveerimisenergiat, mis tuleb ületada, et ainet saaks muuta.




.jpg)